人工イクラ
Aoi Sakata
1 概要
かつて、高価であり鮮度の管理に手のかかる天然イクラの代わりとして (食用として!) 人工イクラが使われていたことがありました。魚卵に似たゼリー状の物質でできており、割合簡単に作ることができます。
2 試薬
| アルギン酸ナトリウム | 1.0 g |
| 塩化カルシウム | 8.0 g |
| 食用色素 | 適量 |
3 操作
1. アルギン酸ナトリウム 1.0 g を水 50 ml に溶かす。これに 食用色素を適量加え着色する。
2. 1. とは別に水 50 ml を用意し、これに塩化カルシウム 8.0 g を溶かす。
3. ピペットを用いてアルギン酸ナトリウム水溶液を塩化カルシウム水溶液に一滴ずつ滴下する。すると本物のイクラによく似た人工イクラができる。
※このイクラは実験として作るので絶対に食べないこと
4 原理と試薬について
この実験で鍵となっている物質はアルギン酸ナトリウムです。この物質はアルギン酸 (alginic acid; alga は〔羅〕で藻の意) のナトリウム塩であり、さらにアルギン酸は D-マンヌロン酸と L-グルロン酸 (それぞれ D-mannuronic acid と L-guluronic acid、いずれ も uronic acid の一種) が直鎖状に重合した物質です (図 1)。さて、アルギン酸ナトリウムを水に溶解させるとカルボキシル基がイオン化して直鎖構造を持つアルギン酸イオンが生じます。このイオンどうしが二価の陽イオンであるカルシウムイオンによって架橋されることで、水に不溶でゲル状のアルギン酸カルシウムが生じます。これを利用して、アルギン酸ナトリウム水溶液の液滴の表面にアルギン酸カルシウムの膜を作ることで人工イクラを得ます。
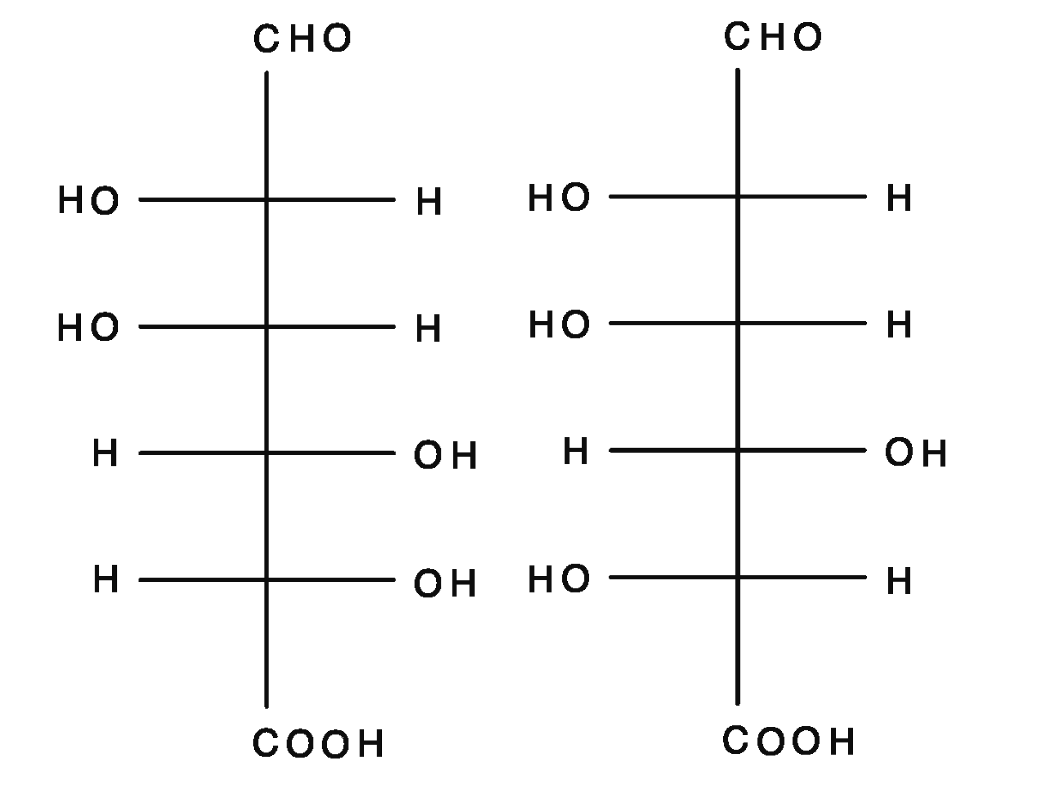
D-マンヌロン酸 L-グルロン酸
図 1 アルギン酸を構成する単糖
アルギン酸イオンをゲル化させるイオンとしては、二価の陽イオンであれば良いので、例えば他にマグネシウムイオンやストロンチウムイオンなどが考えられます。実際、ストロンチウムイオンはカルシウムイオンよりも少量でアルギン酸ストロンチウムのゲルを作ることが知られています。ストロンチウムの放射性同位体は生体に吸収されやすい点で害の多いものであり、アルギン酸の錯体がそうした生体内の放射性ストロンチウムを除去するために投与されることがあります。一方でマグネシウムイオンとアルギン酸イオンの親和性はカルシウムイオンとのものよりも低く、アルギン酸マグネシウムは一部水に溶解します。尚、これらからわかるように、ストロンチウムイオンもマグネシウムイオンもイクラには向きません。
安価な輸入イクラが流通するようになり、保鮮の技術も進歩したため人工イクラは市場から姿を消しました。現在、アルギン酸およびその塩は増粘剤として食品にしばしば使われています。ところが、これらの増粘剤は強塩基などを使わないことにはそのアルギン酸の直鎖を分解できず、廃棄物として見たときには厄介なものです。そこで、アルギン酸はその名の通り天然には海藻類に含まれていることに注目して、海藻類を餌とする生物が持つ、アルギン酸を分解する消化酵素のアルギン酸リアーゼが研究されています。
参考文献
[1] 宮島千尋, 「アルギン酸類の概要と応用」 繊維学会誌 65(12), 2009, p.444-448
[2] 川井正弘、松本孝芳、益田利史郎「二価金属イオンによるアルギン酸水溶液のゲル化に及ぼす添加塩種の影響」日本化学会誌 (化学と工業化学)1993(10), 1993-10-10,p.1184-1187
実験の様子

右の溶液は黄色の色素で着色しています(イクラなのに?)



ピペット(スポイト)を使って黄色の溶液をたらすと、人工イクラができました